Ko stoji iza revolucionarne transplantacije organa i kaže da je ovo tek početak
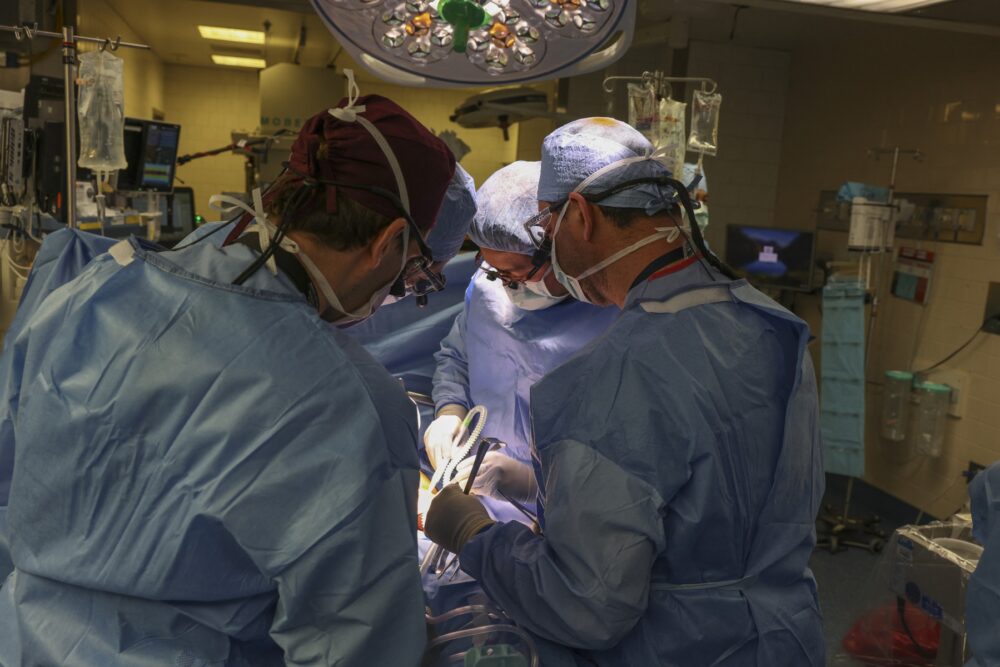
Biotehnološki start-up eGenesis razvio je genetski modificirani bubreg kojeg su prije nekoliko dana uspješno u živog ljudskog pacinenta transprantirali hirurzi Opće bolnice u Massachusettsu.
“Ovaj naučni iskorak znači nadu za desetke ljudi koji svakodnevno umiru čekajući na transplantaciju organa”, rekao je Joren Madsen, direktor transplantacijskog programa na konferenciji za novinare nakon najave zahvata.
“San istraživača na području transplantacije i za njih pravi sveti gral bio je iskoristiti organe svinja kao zamjenu za ljudske organe i tako riješiti problem nedostatka organa”, naglasio je.
Ulazak u novu eru nauke
Naravno, nije bilo tako jednostavno kao samo otići na farmu po bubreg. Razvio ga je startup iz Massachusettsa eGenesis, koji je gotovo desetljeće genetski modificirao organe svinja kako bi se mogli sigurno presaditi u ljude. Ali izvršni direktor Mike Curtis rekao je za Forbes da je prekretnica postignuta ove sedmice samo početak.
Njegova kompanija, koja je dosad prikupila 291 milion dolara rizičnog kapitala, planira klinički testirati svoju tehnologiju za uređivanje gena za transplantaciju bubrega, jetre i srca u sljedeće dvije godine, postajući remetilački igrač na tržištu koje je, prema konsultantskoj kući Grand View vrijedno oko 15 milijardi dolara.
“Pokazali smo da imamo nešto što može pomoći pacijentima”, rekao je. “Za mene je ovo ulazak u novu eru nauke i prilika da pomognem ljudima koji imaju vrlo malo mogućnosti liječenja.”
Trenutno postoji više od 100.000 ljudi na listama čekanja za transplantaciju u Sjedinjenim Državama, ali zbog ograničene dostupnosti doniranih organa, manje od polovine će biti transplantirano u bilo kojoj godini. Decenijama su naučnici mislili da bi životinjski organi mogli pomoći nekim pacijentima, samo da bi pacijente održali na životu dovoljno dugo da prime ljudski organ. Svinje su idealni kandidati za doniranje organa jer brzo rastu, a njihovi su organi po veličini i funkciji slični onima kod ljudi.
U ovom slučaju, pacijent je bio 62-godišnji muškarac kojem prethodna transplantacija bubrega nije uspjela, a postupak se mogao izvesti u okviru Programa proširenog pristupa Uprave za hranu i lijekove (FDA). To omogućuje pacijentima koji su u opasnosti od smrti zbog bolesti da koriste eksperimentalne lijekove ili postupke. Ovaj postupak uslijedio je nakon nekoliko različitih eksperimenata koji su koristili svinjske bubrege kod moždano mrtvih ljudi i dva postupka u kojima su genetski modificirana svinjska srca transplantirana živim pacijentima.
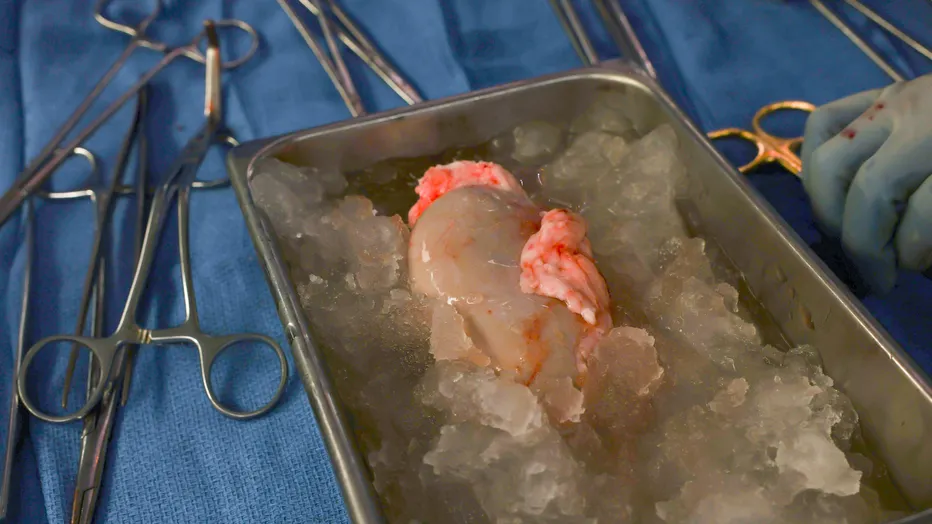
Proboj na koji je medicina čekala desetljećima
Jamil Azzi, transplantacijski hirurg u Brigham and Women's bolnici koji nije bio uključen u operaciju u četvrtak, izrazio je svoje uzbuđenje zbog postupka.
“Ovo je veliki napredak za koji se medicina pripremala decenijama”, rekao je za Forbes. Ipak, upozorio je da će biti potrebno prikupiti mnogo više podataka prije nego što ova vrsta operacije postane rutina za ljudske pacijente.
Ključno pitanje je koliko dugo će svinjski bubreg trajati kod ljudskog pacijenta.
“Ako otkaže za dva do tri mjeseca, još uvijek nismo dovoljno daleko”, rekao je.
Godine 2023. dva pacijenta kojima je presađeno svinjsko srce koje je razvila podružnica United Therapeuticsa Revivicor umrla su nekoliko sedmica nakon operacije, no još uvijek nije sasvim jasno zašto.
Mijenjanje gena
Jedan od najvećih izazova kod presađivanja životinjskog organa u čovjeka je osigurati da tijelo primatelja ne odbaci organ u potpunosti. To već predstavlja problem s bubrezima koje su donirali ljudi, a skeptici su tvrdili da ne postoji način na koji bi takva transplantacija uspjela zbog mnogih razlika između svinja i ljudi.
Ovdje dolazi do preuređivanja gena. Curtis je objasnio da je operacija prošle sedmice zahtijevala genetsku modifikaciju svinjskog bubrega sa sedam različitih ljudskih gena, uklanjanje tri svinjska gena i 59 dodatnih dijelova DNK. Ove promjene osiguravaju da imunološki sistem pacijenta neće napasti bubreg do te mjere da ga odbaci, iako su imunosupresivni lijekovi potrebni, baš kao i kod ljudskih organa.

Te su promjene napravljene u jednoj svinjskoj stanici, koja je zatim umetnuta u embrij i klonirana. Klonirani embriji zatim su implantirani u krmaču koja je okotila genetski modificirane praščiće. Curtis pojašnjava da s tako velikim brojem promjena raste rizik od nenamjerne promjene drugih dijelova genoma životinje, što oni nazivaju “promjenama izvan cilja”.
Ali u proteklih nekoliko godina, napredak u sekvencioniranju genoma omogućio je utvrđivanje jesu li se dogodile promjene izvan cilja. U slučaju ove svinje, eGenesis je uspio utvrditi da su takve promjene bile minimalne i da ne bi imale nikakav učinak na rezultat.
Potrebno je više eksperimenata na primatima
U članku objavljenom prošle jeseni u časopisu Nature, eGenesis je opisao slučajeve u kojima su majmuni kojima su presađeni svinjski bubrezi preživjeli više od godinu, a u jednom slučaju više od dvije godine. Curtis je rekao da je na temelju ovih podataka i ovogodišnje uspješne transplantacije bubrega njihova firma toliko napredovala da će već 2025. godine moći službeno podnijeti zahtjev FDA-i za početak potpunog kliničkog ispitivanja transplantacije višestrukih svinjskih bubrega u ljude.
Ali još nisu tamo. Curtis je rekao da agencija želi vidjeti više podataka o ispitivanjima na primatima prije nego što im da zeleno svjetlo. I dok im još treba više podataka, Azzi je dodao da su dosadašnji dokazi dobar pokazatelj da je eGenesis na pravom putu.
Curtis je naglasio da će kompanija, kako bi se povećala, morati moći uzgajati svinje s organima koji su već spremni za doniranje, umjesto da ih moraju klonirati i implantirati. George Church, suosnivač eGenesisa i genetički istraživač na Medicinskom fakultetu Harvarda, rekao je za Forbes da bi ovo moglo osigurati da jedan darivatelj svinje pacijentima osigura više organa.
Naša krajnja vizija je proizvesti organe svinja koji ne zahtijevaju imunosupresiju.Mike Curtis, izvršni direktor eGenesisa
Krajem godine klinička ispitivanja s jetrom
Prema Curtisu, oni su bliže realizaciji programa za genetsku modifikaciju svinjskih jetara i srca za transplantaciju u ljude, koristeći proces sličan onom koji se koristi za bubrege. U januaru su objavili da su izveli uspješnu operaciju genetski modificirane svinjske jetre kod moždano mrtvog pacijenta, pri čemu je donirani organ spojen vantjelesno. Ovaj bi postupak mogao pomoći pacijentima sa zatajenjem jetre da prežive nekoliko ključnih dana – dovoljno dugo da se pronađe ljudski donor.
Budući da su bili toliko uspješni, Curtis je rekao da planiraju podnijeti zahtjev FDA-i za korištenje genetski modificirane jetre i započeti klinička ispitivanja do kraja ove godine. Naposljetku, žele da se njihova jetra u potpunosti transplantira živim pacijentima.
Djeca u prvom planu
Cilj eGenesisa je trajna transplantacija bubrega i jetre. Kod programa za srce, Curtis kaže da su prvenstveno fokusirani na pedijatrijske pacijente, za koje bi svinjsko srce moglo biti učinkovit most dok ne dobiju ljudski organ. Prema njegovim riječima, trenutno više od polovine djece kojoj je potrebno novo srce umire čekajući transplantaciju.
U sklopu pokusa, pavijani s genetski modificiranim srcem preživjeli su više od 200 dana, a Curtis se nada da bi to moglo dovesti do napretka u naporima za presađivanje srca kod djece, bilo kasnije ove ili početkom sljedeće godine.
Dugoročno, eGenesis ima još veće ambicije.
“Krajnja vizija je proizvesti svinjske organe koji ne bi zahtijevali imunosupresiju”, rekao je Curtis.
To bi moglo značiti da pacijenti nakon transplantacije ne bi trebali uzimati lijekove koji usporavaju imunološki sistem kako bi spriječili odbacivanje.
To ih održava na životu, ali ih istovremeno izlaže većem riziku od infekcije i raka.
“Znamo da će to zahtijevati dodatno inženjerstvo, ali trebat će nam podaci o toku i uspjehu ovih vrsta operacija kod ljudi kako bismo odredili kakav će to inženjering biti.”
Sljedeći korak “poboljšani organi”?
Genetičar George Church, suosnivač eGenesisa, dodao je da bi moć genetskog inženjeringa mogla jednog dana omogućiti firmi da stvori “poboljšane organe” uz organe za koje transplantirani pacijenti neće morati uzimati lijekove.
Na primjer, bilo bi moguće modificirati genome svinja kako bi se stvorili organi otporni na mnoge patogene ili čak organi koji sporije stare, rekao je. Kao dokaz za ovaj koncept naveo je istraživanje iz svog laboratorija na Harvard Medical School, čiji su recenzirani rezultati objavljeni u časopisu Nature. Jednostavnom genetskom promjenom napravili su bakterijsku vrstu otpornu na sve poznate viruse.
“Sada to želimo učiniti sa svinjama”, rekao je.
U bliskoj budućnosti, eGenesis će morati povećati poslovanje, što će također zahtijevati više kapitala, rekao je Curtis. Trenutno ga imaju dovoljno za rad do kraja 2026. godine i, rekao je, već prikupljaju dodatna sredstva. Curtis se nada da će uspješna operacija potencijalnim investitorima pokazati da su na pravom putu.
“Ova prva transplantacija bubrega živoj osobi potvrđuje cijeli naš pristup”, rekao je i dodao: “A to će nam omogućiti ne samo da znamo kako pripremiti bubrege za transplantaciju, već uskoro i jetru i srce.”
Autor: Alex Knapp, Forbes






